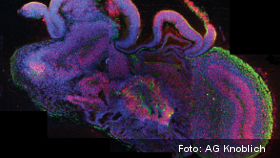
Ziemlich einzigartig
(26.09.2019) Mit Hirn-Organoiden Medikamente gegen Epilepsie finden, das ist der Plan der frischgegründeten a:head bio AG. Mitgründer ist Organoid-Pionier Jürgen Knoblich.
Als 2013 der Durchbruch zu den Hirn-Organoiden gelang, war es schon eine große Sensation. Aus embryonalen oder induzierten pluripotenten Stammzellen war es gelungen, Hirn-ähnliche Mikrostrukturen zu erzeugen, die sich als Zellkultur-Modelle für das menschliche Groß und Kleinhirn eignen. In einem Nature-Paper beschrieb das Team um Madeline Lancaster und Jürgen Knoblich, beide damals am Wiener Institut für Molekulare Biotechnologie (IMBA), das dazugehörige Protokoll, mit dem man etwa vier Millimeter große Organoide in etwa zwei Monaten im Inkubator heranzüchten konnte. Mehr als tausend Zitierungen sammelte das Protokoll seither, und wurde in der Zwischenzeit von Knoblichs Labor und vielen anderen weiterentwickelt.
Ihre einzigartige Expertise wollen die Österreicher jetzt nutzen, um Medikamente für Patienten mit neurologischen Erkrankungen zu entwickeln – natürlich mithilfe der Organoide. Hierfür gründeten sie die a:head bio AG, das erste Unternehmen weltweit, das sich an solch komplexe Modelle herantraut.
Aufwendige Produktion
Denn die Herstellung der Organoide ist sehr aufwendig: Man nimmt pluripotente Stammzellen und kultiviert sie in Suspension für sechs Tage, währenddessen bilden sie die sogenannten „embryoid bodies”. Man gibt diesen „neural induction medium“ für weitere fünf bis sieben Tage und schließt sie dann in einen Tropfen Matrigel ein, in Differenzierungsmedium. Dann werden sie in Suspension geschüttelt, und schon wachsen die kleinen Klumpen zu ausgereiften Hirn-Organoiden heran. Diese bilden sogar unterschiedliche Hirn-Regionen ab, wie Vorder- und Kleinhirn, und die gebildeten Zellen funktionieren nachweislich wie Neuronen im menschlichen Cortex. Mit den Organoiden lassen sich sogar neurologische Entwicklungsstörungen modellieren, wie etwa Mikrozephalie: hier fallen die Organoide kleiner aus als die der Kontrollgruppe.
Ihre Erfindungen haben die Forscher am IMBA stets schleunigst patentieren lassen, sodass sie diese jetzt auf die nächste Stufe heben können und kommerzialisieren. Jürgen Knoblich ist nun nicht mehr nur Leiter seiner Arbeitsgruppe und Direktor des IMBA, sondern auch Gründer. „Das IMBA ist ein Grundlagen-Institut, aber sehr offen für Anwendungen. Wir haben eine ’translational research unit’, um unsere Technologien in die Anwendung zu übersetzen. Und das haben wir nun mit den Hirn-Organoiden getan.“ Kräftige Unterstützung mit Kapital kam von einer Wiener Beteiligungsgesellschaft, die mit einem siebenstelligen Betrag eingestiegen ist. Zurzeit ist das Spin-off noch am IMBA angesiedelt, wird aber bald in einen Inkubator im Nebengebäude umziehen.
Schulung inklusive
Oliver Szolar, Biotechnloge mit Geschäftsführer-Erfahrung, ist CEO von a:head bio und gerade auch fleißig dabei, Mitarbeiter einzustellen, die anschließend in der Organoid-Technologie geschult werden. Dafür nutzt er den engen Kontakt zu Knoblichs Labor, wie dieser uns erklärt: „Die Firma fängt ja gerade erst an, wir haben einen Kooperationsvertrag über drei Jahre, um die Firma auf den Weg zu bringen. Die Angestellten der Firma werden von uns in der Organoid-Technologie trainiert.“ Die Schöpfer der Organoid-Technologie halten sich nämlich aus dem operativen Geschäft des Spin-offs heraus, sie sitzen jedoch im „advisory board“. Madeline Lancaster hat übrigens längst ihre eigene Gruppe am MRC Laboratory of Molecular Biology in Cambridge, UK.
Und was hat a:head bio nun in den nächsten Jahren vor? Zunächst wird die Firma humane induzierte pluripotente Stammzellen (hiPSC) von gesunden und kranken Spendern verwenden, wie Knoblich erklärt. „Wir wollen Organoid-Modelle mit neurologischen Erkrankungen herstellen, angefangen haben wir mit Epilepsie. Wir versuchen, die Epilepsie im Organoid-Modell nachzustellen. Unser Ziel ist es, den Maßstab zu erhöhen, sodass man Medikamenten-Screenings durchführen kann.“
Dazu entwickeln die Forscher Assays, die im Hochdurchsatz machbar sind. Es gibt tatsächlich viele solcher Assays – welche genau sie benutzen, kann Knoblich uns natürlich nicht verraten. Ein Beispiel sind jedoch optogenetische Verfahren, um neuronale Aktivität mit Fluoreszenz sichtbar zu machen.
Zunächst wird die Firma bereits zugelassene Medikamente testen. Schlagen die Epilepsie-Organoid-Modelle darauf an, sind die Assays verifiziert. Im zweiten Schritt will die Firma neue Wirkstoffe testen, um bessere Medikamente gegen Epilepsie zu finden.
Beginn einer Revolution
Wenn die Technologie funktioniert, wird das eine ziemliche Revolution auslösen, ist Knoblich überzeugt. „Der Stand in der Epilepsie-Forschung heutzutage ist immer noch der, dass Medikamente am Mausmodell entwickelt werden, mit genetisch induzierten Epilepsien. Wir werden diese ablösen können, mit hiPSC-Linien von Epilepsie-Patienten.“ Ein weiterer großer Vorteil der Methode: Die meisten Epilepsie-Fälle beruhen nicht auf bekannten Mutationen, sondern sind unbekannter Natur. „Und diese Fälle werden wir als Tests nehmen können, denn auch von diesen Patienten können wir hiPSCs gewinnen und im Organoid-Modell mit Wirkstoffen testen”.
Neue Epilepsie-Medikamente werden in der Tat dringend gebraucht. „Es gibt Epilepsie-Medikamente und die funktionieren auch bei einigen Patienten, aber bei den meisten funktionieren sie eben nicht“, verdeutlicht Knoblich. Und da spricht er das große Problem der Pharma-Branche an: Das letzte zugelassene Epilepsie-Medikament basiert auf einem Cannabis-Inhaltsstoff. Offensichtlich fällt den Firmen nichts Neues mehr ein. „Nicht nur ich, sondern die ganze Branche macht sich mit den Zellmodellen große Hoffnung. Sie werden diese Forschung sicher revolutionieren.“
Das Wachstum der a:head bio AG hat Knoblich auch schon im Blick: „Die Firma ist ja gerade erst gegründet worden und die ersten Leute werden eingestellt, aber mit zwei oder drei Forschern kommen wir nicht weit. Das Ganze ist schon sehr arbeitsintensiv, und ich hoffe schon, dass die Firma sehr schnell wachsen wird.“
Karin Lauschke