Zyklosom
von Petra Stöcker (Laborjournal-Ausgabe 7, 2009)
Die „Standard Operation Procedure“ der Zellteilung eukaryotischer Organismen sieht vor, dass die Chromosomen verdoppelt und jeweils ein Schwesterchromatid auf die beiden neu entstehenden Tochterzellen verteilt wird.
Bei diesem Vorgang durchlaufen alle teilungswütigen Zellen wohlgeordnet und zeitlich abgestimmt den Zellzyklus. Die Basisorganisation des Zellzyklus ist in allen Eukaryoten die gleiche. So kann man zum Beispiel Zellzyklusproteine eines Säugers in eine Hefezelle umsiedeln, und die Proteine arbeiten auch dort.
Zellzyklus
Man unterscheidet zwei Phasen des Zellzyklus: die Interphase, die den größten zeitlichen Anteil des Zellzyklus ausmacht, und die Mitose, beginnend mit dem Wachstum der Zellen und Verdopplung der Chromosomen und mit der Teilung von Mutter- und Tochterzelle endend.
Die Interphase wird in drei Abschnitte unterteilt: die G1 (Gap1)-, die S (Synthese)- und die G2 (Gap2)-Phase. Die G1-Phase als Wachstumsphase schließt sich an eine Zellteilung (Mitose) an. Es folgt die Synthesephase, in der die DNA der Zelle repliziert wird.
In der G2-Phase bereitet sich die Zelle mit weiterem Wachstum und Proteinbiosynthese auf die nächste Mitose vor und prüft, ob die Replikation vollständig und fehlerfrei abgelaufen ist. Ist das nicht der Fall, findet keine Zellteilung statt.
Chromosomenaufteilung
Bei der Mitose wird’s spannend. Der Zellzyklus läuft ja streng kontrolliert und geordnet ab und daher ist auch die Mitose – wen wundert’s – in Schritte unterteilt: In der Prophase werden die Chromosomen kondensiert. Die Schwesterchromatiden, also Kopie und Original, sind am Zentromer noch miteinander verbunden.
In der Metaphase ordnen sich die Chromatiden im Zentrum der Zelle an der so genannten „Metaphaseplatte“ an und die Kernspindeln werden ausgebildet. Sie setzen am Kinetochor-Proteinkomplex des Zentromers an.
In der Anaphase werden die Schwesterchromatiden durch die Spindelfasern zu den entgegengesetzten Spindelpolen der entstehenden Tochterzellen transportiert und auf die zwei künftigen Kerne verteilt. Dieser Vorgang wird in der Telophase abgeschlossen, der Kern teilt sich.
Mitoseregulation
Die Aktivitäten der zahlreichen, an der DNA-Synthese und der Mitose beteiligten Proteine werden von einer Handvoll heterodimerer Proteinkinasen reguliert. Die regulatorischen Untereinheiten dieser Proteinkinasen bezeichnet man als Cycline, da ihr Gehalt im Verlauf des Zellzyklus in charakteristischer Weise zu- und abnimmt.
Die katalytischen Untereinheiten sind Cyclin-abhängige Kinasen, sie werden erst nach Andocken an ein Cyclin als Kinasen aktiv. Die Proteinkinasen aktivieren beziehungsweise blockieren regulatorische Einheiten von Zellzyklusproteinen durch Phosphorylierung. Sie stimmen also die Proteinarbeit und damit auch den Zellzyklus zeitlich ab.
Cycline aktivieren auch den Anaphase-fördernden Komplex (anaphase-promoting complex, APC), das Zyklosom. Dieser Multiproteinkomplex wiederum – nun wachgerüttelt – heftet an Hemmstoffe der Anaphase Ubiquitinreste an und verdammt sie damit zur Proteolyse.
In Reih‘ und Glied
Zu den bekanntesten Zyklosom-Substraten zählen Cyclin-B und Securin, Proteine des Übergangs der Meta- in die Anaphase. Mit ihrer Ubiqitinylierung ist der Startschuss für die Anaphase gefallen. Erst jetzt wird die Kohäsion der Schwesterchromatiden gelöst und sie können zu den gegenüberliegenden Spindelpolen gezogen werden.
Das Zyklosom ist damit der Hauptregulator des zeitlichen Ablaufs der Mitose. Er setzt ein, wenn alle Chromosomen hübsch nach Plan aufgereiht in der Zellmitte mit den Spindelfasern verbunden sind.
Tanzt auch nur eines der Chromosomen aus der Reihe und ist nicht sachgerecht oder gar nicht mit dem Spindelapparat verbunden, hat eine Chromatidenaufteilung schwerwiegende Folgen: Es kommt zu Fehlverteilungen, was wiederum eine Tumorbildung auslösen kann. So ist die fehlende Kontrolle des Zellzyklus ein Charakteristikum von Krebszellen.
Anhänglicher Checkpoint
Bei der Chromatidenaufteilung wird daher ein Helferlein tätig, welches Wissenschaftler am Forschungsinstitut für Molekulare Pathologie in Wien, am Max-Planck-Institut für Biophysikalische Chemie in Göttingen und am European Molecular Biology Laboratory (EMBL) in Heidelberg charakterisiert haben (Science 323:1477-81).
Solange nicht alle Chromosomen mit ihrem Zentromer korrekt an Spindelfasern geknüpft sind, klammert sich ein so genannter „mitotic checkpoint complex“ (MCC) an das Zyklosom. MCC kuschelt sich in die Tasche, mit der das Zyklosom an sein Substrat (Cyclin B sowie Securin) bindet, und verhindert so deren Ubiqitinylierung – die Anaphase muss warten.
MCC wird in der Prometaphase aktiviert durch Anwesenheit von freien Kinetochor-Proteinkomplexen des Zentromers, die nicht ordentlich an Spindelfasern geknüpft sind.
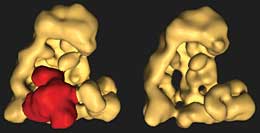
Mit elektronenmikroskopischen Techniken erkannten die Forscher, dass die Bindung von MCC das Zyklosom zu einer Konformationsänderung veranlasst: es friert in einer geschlossenen Konformation ein. Die Chromosomen werden nicht aufgeteilt.
Letzte Änderungen: 30.07.2009